《(遵義專用)2019中考化學高分一輪復習 第1部分 教材系統(tǒng)復習 第6章 溶解現(xiàn)象真題精練》由會員分享,可在線閱讀����,更多相關(guān)《(遵義專用)2019中考化學高分一輪復習 第1部分 教材系統(tǒng)復習 第6章 溶解現(xiàn)象真題精練(4頁珍藏版)》請在裝配圖網(wǎng)上搜索。
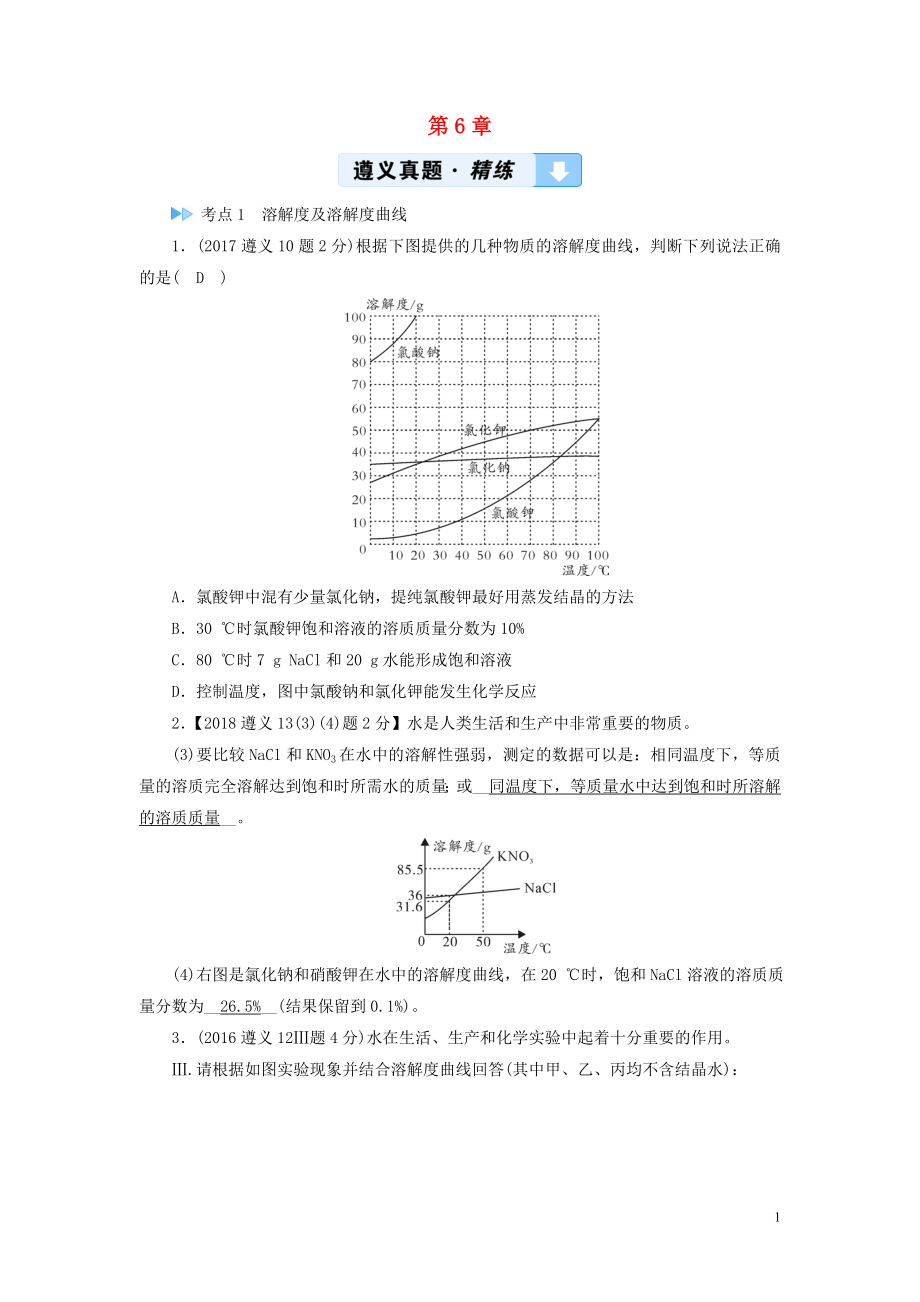
1�����、第6章 考點1溶解度及溶解度曲線1(2017遵義10題2分)根據(jù)下圖提供的幾種物質(zhì)的溶解度曲線����,判斷下列說法正確的是(D)A氯酸鉀中混有少量氯化鈉��,提純氯酸鉀最好用蒸發(fā)結(jié)晶的方法B30 時氯酸鉀飽和溶液的溶質(zhì)質(zhì)量分數(shù)為10%C80 時7 g NaCl和20 g水能形成飽和溶液D控制溫度��,圖中氯酸鈉和氯化鉀能發(fā)生化學反應2【2018遵義13(3)(4)題2分】水是人類生活和生產(chǎn)中非常重要的物質(zhì)��。(3)要比較NaCl和KNO3在水中的溶解性強弱�����,測定的數(shù)據(jù)可以是:相同溫度下�����,等質(zhì)量的溶質(zhì)完全溶解達到飽和時所需水的質(zhì)量��;或_同溫度下��,等質(zhì)量水中達到飽和時所溶解的溶質(zhì)質(zhì)量_����。(4)右圖是氯化鈉和硝酸鉀
2��、在水中的溶解度曲線,在20 時����,飽和NaCl溶液的溶質(zhì)質(zhì)量分數(shù)為_26.5%_(結(jié)果保留到0.1%)。3(2016遵義12題4分)水在生活����、生產(chǎn)和化學實驗中起著十分重要的作用。.請根據(jù)如圖實驗現(xiàn)象并結(jié)合溶解度曲線回答(其中甲�����、乙�����、丙均不含結(jié)晶水):(1)生石灰與水反應的化學方程式為_CaOH2O=Ca(OH)2_��,試管內(nèi)所盛飽和溶液的溶質(zhì)為對應溶解度曲線中的_丙_(填“甲”“乙”或“丙”)��。(2)如果要配制相同濃度的甲��、乙飽和溶液����,需要把溫度控制在_t2_。(3)t3 時��,將甲��、乙�����、丙的飽和溶液都降溫到t1 ��,溶液中溶質(zhì)質(zhì)量分數(shù)由小到大的順序為_丙甲乙_��。4(2015遵義14題4分)溶解度是解
3����、決溶液相關(guān)問題的重要依據(jù)。.根據(jù)右圖解決下列問題:(M����、N均不含結(jié)晶水)(1)溫度為_t2_時,M��、N兩種物質(zhì)的溶解度相等��。(2)t1 時��,將20 g M加入50 g 水中,充分溶解����,形成溶液的質(zhì)量為_65_g,保持溫度不變����,向該溶液中再加入10 g水充分攪拌,溶液的溶質(zhì)質(zhì)量分數(shù)將_不變_(填“變大”“不變”或“變小”)����。(3)t2 時,將25 g N加入50 g水中����,完全溶解后要提高該溶液的溶質(zhì)質(zhì)量分數(shù),其操作方法是_降低溫度并加入固體N_����。5【2014遵義13(1)題4分】水是重要的物質(zhì)��,在實驗室中常用于溶解物質(zhì)����、配制溶液。(1)向50 mL水(密度為1 g/mL)中溶解一定量KNO3固體
4、的操作如下��,請根據(jù)下圖實驗現(xiàn)象和溶解度曲線回答����。A、B����、C中一定是飽和溶液的是_B_,一定是不飽和溶液的是_A_(填字母)����;當x_5.8_g時,B中恰好沒有固體剩余�����;硝酸鉀從溶液中析出晶體常用_降溫結(jié)晶(或冷卻熱飽和溶液)_的方法����。 考點2配制一定溶質(zhì)質(zhì)量分數(shù)的NaCl溶液6【2018遵義13(2)題2分】水是人類生活中非常重要的物質(zhì)。(1)水是一種常見的溶劑?���,F(xiàn)需要配制500 g溶質(zhì)質(zhì)量分數(shù)為15%的食鹽溶液用于農(nóng)業(yè)選種��,操作過程是:計算得出需要食鹽的質(zhì)量是_75_g����;稱量操作的先后順序是_BA_(填序號)��。A在天平的左盤放入所需的食鹽B在天平的右盤放入所需的砝碼7【2014遵義13(2)題
5�����、3分】水是重要的物質(zhì)��,在實驗室中常用于溶解物質(zhì)����、配制溶液。(2)根據(jù)下列儀器��,欲配制一定質(zhì)量分數(shù)的食鹽溶液��,回答下列問題��。,A),B),C),D),E),F),G)上面的儀器中除D�����、E外�����,還必須選用的儀器有_BG_(填字母)��;E的作用是_攪拌����、加速溶解_,配制的步驟可以概括為計算�����、稱取�����、量取�����、_溶解_��、裝瓶�����、貼標簽。 考點3粗鹽提純 8【2015遵義14(2)題2分】溶解度是解決溶液相關(guān)問題的重要依據(jù)�����。.根據(jù)下表解決實際問題:溫度/2030506080溶解度/gKNO331.645.885.5110169K2CO3110114121126139某KNO3樣品中含有少量K2CO3��,其提純過程如下:(1)上圖中溶液C是_飽和_(填“飽和”或“不飽和”)溶液�����。(2)樣品中鉀元素的質(zhì)量為_33_g(結(jié)果保留整數(shù))��。 考點4溶質(zhì)質(zhì)量分數(shù)相關(guān)的計算9(2015遵義18題4分)為了測定某稀硫酸的溶質(zhì)質(zhì)量分數(shù)��,在10 g稀硫酸中滴加過量的氯化鋇溶液����,得到沉淀2.33 g,求該稀硫酸的溶質(zhì)質(zhì)量分數(shù)�����。解:設稀硫酸中的溶質(zhì)質(zhì)量為x。H2SO4BaCl2= BaSO42HCl98233x 2.33 gx0.98 g稀硫酸中的溶質(zhì)質(zhì)量分數(shù)為100%9.8%�����。答:該稀硫酸中溶質(zhì)的質(zhì)量分數(shù)為9.8%����。4
 (遵義專用)2019中考化學高分一輪復習 第1部分 教材系統(tǒng)復習 第6章 溶解現(xiàn)象真題精練
(遵義專用)2019中考化學高分一輪復習 第1部分 教材系統(tǒng)復習 第6章 溶解現(xiàn)象真題精練