《湖南省株洲縣祿口鎮(zhèn)中學九年級化學下冊《第九單元 課題3 溶液的濃度》學案1(無答案)(新版)新人教版》由會員分享�����,可在線閱讀��,更多相關(guān)《湖南省株洲縣祿口鎮(zhèn)中學九年級化學下冊《第九單元 課題3 溶液的濃度》學案1(無答案)(新版)新人教版(2頁珍藏版)》請在裝配圖網(wǎng)上搜索����。
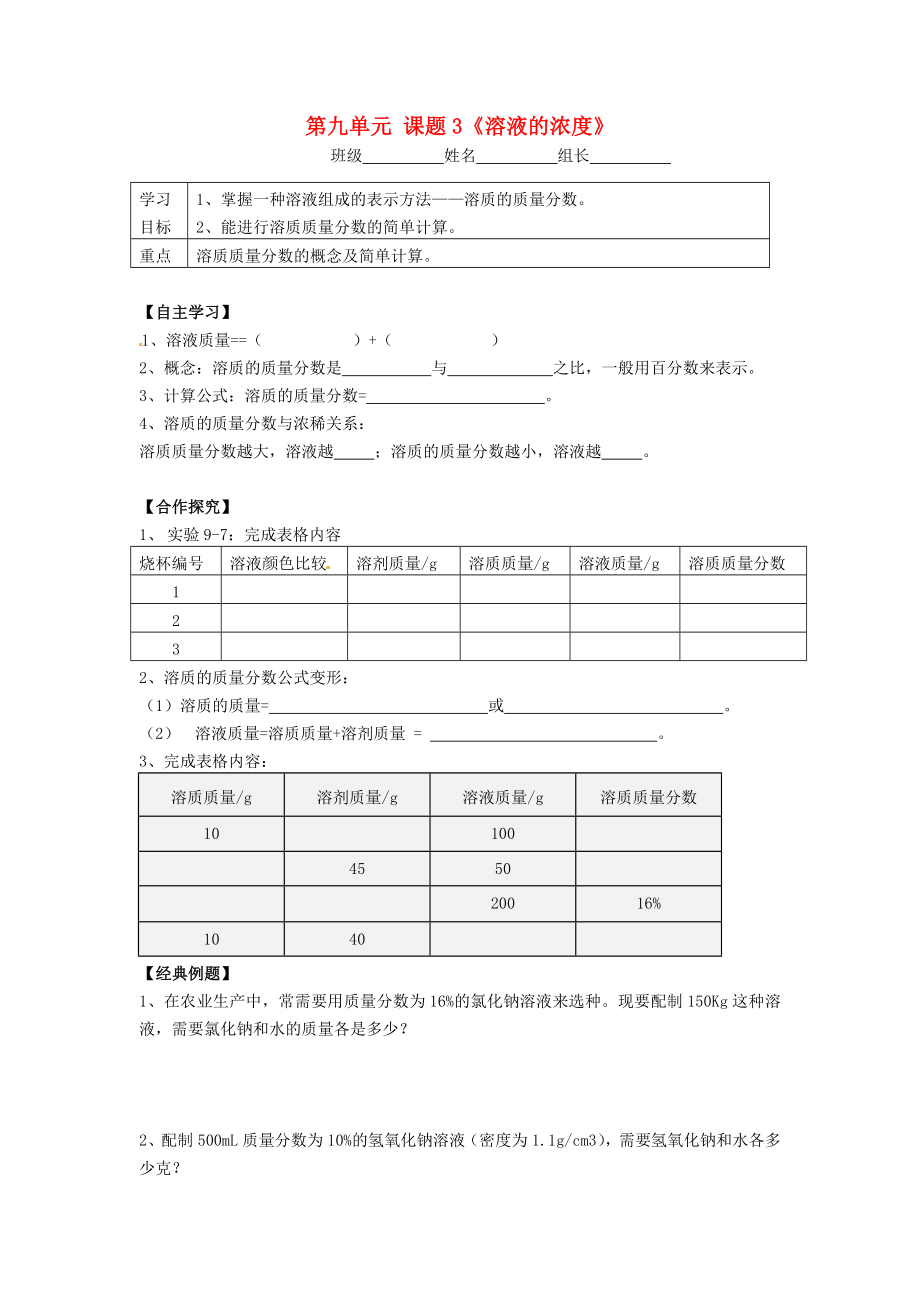
1�����、第九單元 課題3溶液的濃度班級姓名組長 學習目標1��、掌握一種溶液組成的表示方法溶質(zhì)的質(zhì)量分數(shù)。2���、能進行溶質(zhì)質(zhì)量分數(shù)的簡單計算�。重點溶質(zhì)質(zhì)量分數(shù)的概念及簡單計算�����?!咀灾鲗W習】1、溶液質(zhì)量=( )+( )2�����、概念:溶質(zhì)的質(zhì)量分數(shù)是 與 之比�,一般用百分數(shù)來表示。3�����、計算公式:溶質(zhì)的質(zhì)量分數(shù)= ��。4����、溶質(zhì)的質(zhì)量分數(shù)與濃稀關(guān)系:溶質(zhì)質(zhì)量分數(shù)越大����,溶液越 �����;溶質(zhì)的質(zhì)量分數(shù)越小��,溶液越 ����。【合作探究】1�、 實驗9-7:完成表格內(nèi)容 燒杯編號溶液顏色比較溶劑質(zhì)量/g溶質(zhì)質(zhì)量/g溶液質(zhì)量/g 溶質(zhì)質(zhì)量分數(shù)1232、溶質(zhì)的質(zhì)量分數(shù)公式變形:(1)溶質(zhì)的質(zhì)量= 或 �。(2) 溶液質(zhì)量=溶質(zhì)質(zhì)量+溶劑質(zhì)量 = 。
2�、3、完成表格內(nèi)容:溶質(zhì)質(zhì)量/g溶劑質(zhì)量/g溶液質(zhì)量/g溶質(zhì)質(zhì)量分數(shù)10100455020016%1040【經(jīng)典例題】1����、在農(nóng)業(yè)生產(chǎn)中���,常需要用質(zhì)量分數(shù)為16%的氯化鈉溶液來選種?,F(xiàn)要配制150Kg這種溶液,需要氯化鈉和水的質(zhì)量各是多少��?2�����、配制500mL質(zhì)量分數(shù)為10%的氫氧化鈉溶液(密度為1.1g/cm3)�,需要氫氧化鈉和水各多少克?【體驗成功】A級 1���、某溫度時�����,蒸干40克氯化鉀溶液��,得到8克氯化鉀���,求該溶液中溶質(zhì)的質(zhì)量分數(shù)。B級2���、若用200毫升15%的氯化鈉溶液(密度為1.5克/毫升)來選種�����,則需要水和氯化鈉的質(zhì)量各是多少����?3、 在20時���,要提純50克含有少量泥沙的粗鹽����,最好用多少克水來溶解粗鹽(20時����,食鹽的溶解度為36克)?C級 4�����、將30gNaCl放入270g水中���,全部溶解后,溶質(zhì)質(zhì)量為 �����,溶劑質(zhì)量為 ���,溶液質(zhì)量為 ,溶液的質(zhì)量分數(shù)為 若將其升溫到40時�����,溶質(zhì)的質(zhì)量分數(shù)為 ���;若將得到的溶液分成三等份��,則每一份溶液質(zhì)量為 ����,溶質(zhì)的質(zhì)量分數(shù)為 ���。第份溶液中蒸發(fā)克水��,這樣形成的不飽和溶液中溶質(zhì)質(zhì)量分數(shù)為多少��?第份溶液加入克水�����,這樣形成溶液的質(zhì)量分數(shù)為多少�����?第份加入克NaCl����,這樣形成的不飽和溶液中溶質(zhì)質(zhì)量分數(shù)為多少��?我學會了: 我的疑惑:
 湖南省株洲縣祿口鎮(zhèn)中學九年級化學下冊《第九單元 課題3 溶液的濃度》學案1(無答案)(新版)新人教版
湖南省株洲縣祿口鎮(zhèn)中學九年級化學下冊《第九單元 課題3 溶液的濃度》學案1(無答案)(新版)新人教版