《高中化學(xué)專題一 化學(xué)家眼中的物質(zhì)世界課件 蘇教版必修一原子結(jié)構(gòu)第一課時》由會員分享��,可在線閱讀���,更多相關(guān)《高中化學(xué)專題一 化學(xué)家眼中的物質(zhì)世界課件 蘇教版必修一原子結(jié)構(gòu)第一課時(31頁珍藏版)》請在裝配圖網(wǎng)上搜索��。
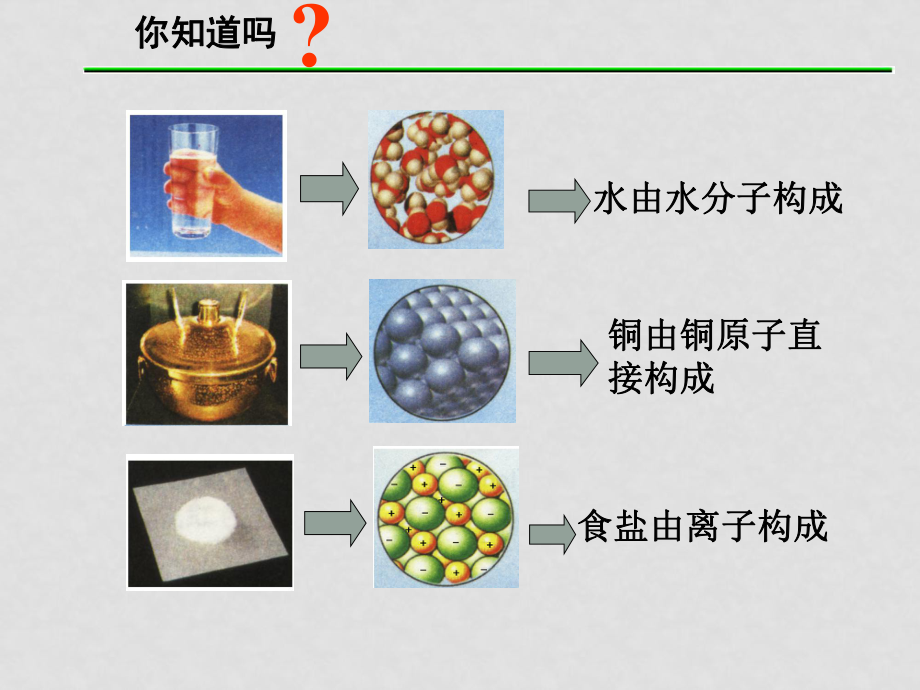
1�、水由水分子構(gòu)成水由水分子構(gòu)成銅由銅原子直銅由銅原子直接構(gòu)成接構(gòu)成食鹽由離子構(gòu)成食鹽由離子構(gòu)成你知道嗎你知道嗎?一�����、原子結(jié)構(gòu)模型的演變一、原子結(jié)構(gòu)模型的演變 湯姆生原子模型(湯姆生原子模型(1904年):年):盧瑟福原子模型(盧瑟福原子模型(1911年):年):波爾波爾原子模型原子模型(1913年年):現(xiàn)代原子模型現(xiàn)代原子模型:道爾頓原子模型(道爾頓原子模型(1803年):年): 原子是原子是實心球?qū)嵭那颉捌咸迅擅姘狡咸迅擅姘健痹咏Y(jié)構(gòu)模型原子結(jié)構(gòu)模型帶核的帶核的原子結(jié)構(gòu)模型原子結(jié)構(gòu)模型分層分層模型模型電子云電子云模型模型1 1��、實驗方法是科學(xué)研究的一種重要方法����。、實驗方法是科學(xué)研究的一種重
2�、要方法。2 2����、科學(xué)研究、科學(xué)發(fā)現(xiàn)是永無止境的�、科學(xué)研究����、科學(xué)發(fā)現(xiàn)是永無止境的電子層數(shù)電子層數(shù) 一一 二二 三三 四四 五五 六六 七七電子符號電子符號 K L M N O P Q電子能量電子能量 低低 高高離核距離離核距離 近近 遠(yuǎn)遠(yuǎn)1、電子層���、電子層+15第第1層層第第2層層第第3層層K層層L層層M層層原子核原子核原子核帶正電原子核帶正電核電荷數(shù)核電荷數(shù)285二、原子結(jié)構(gòu)示意圖二����、原子結(jié)構(gòu)示意圖 為了為了形象地形象地表示原子的結(jié)構(gòu)���,人們就創(chuàng)表示原子的結(jié)構(gòu),人們就創(chuàng)造了造了“原子結(jié)構(gòu)示意圖原子結(jié)構(gòu)示意圖”這種特殊的圖形�。這種特殊的圖形。每個電子層最多只能容納每個電子層最多只能容納2n2個電子
3��、����。個電子����。 最外層最多只能容納最外層最多只能容納 8個電子個電子 (K層為最外層時不能超過層為最外層時不能超過2個)個) 次外層最多只能容納次外層最多只能容納18個電子個電子 (K層為次外層時不能超過層為次外層時不能超過2個)個) 倒數(shù)第三層最多只能容納倒數(shù)第三層最多只能容納32個電子個電子 先排先排K層,排滿層��,排滿K層后再排層后再排L層,排滿層���,排滿L層后層后 再排再排M層層注意:多條規(guī)律必須同時兼顧。注意:多條規(guī)律必須同時兼顧����。 請同學(xué)們畫出下列原子的結(jié)構(gòu)示意圖請同學(xué)們畫出下列原子的結(jié)構(gòu)示意圖練一練練一練:H O Mg Cl Ca核電核電核數(shù)核數(shù)元素元素名稱名稱元素元素符號符號各電子層的
4、電子數(shù)各電子層的電子數(shù)KLMNOP2氦氦He2 10氖氖Ne28 18氬氬Ar288 36氪氪Kr28188 54氙氙Xe2818188 86氡氡Rn2818321884 4��、原子結(jié)構(gòu)與元素性質(zhì)的關(guān)系��、原子結(jié)構(gòu)與元素性質(zhì)的關(guān)系(結(jié)構(gòu)決定性質(zhì))(結(jié)構(gòu)決定性質(zhì))(1 1)穩(wěn)定結(jié)構(gòu)穩(wěn)定結(jié)構(gòu): (如(如HeHe�、NeNe����、ArAr等)等)即最外層為即最外層為8電子的結(jié)構(gòu)(電子的結(jié)構(gòu)(K層為層為2個)個)特點:原子既不容易失去電子又不特點:原子既不容易失去電子又不容易得到電子容易得到電子+2He+18Ar+10Ne該電子層該電子層上的電子上的電子失去電子+12282Mg+1228Mg2+得到電子+826
5、O+828O2- 原子最外層的電子數(shù)小于原子最外層的電子數(shù)小于8個時�����,在個時�����,在化學(xué)反應(yīng)中總是得到或失去電子而達(dá)到化學(xué)反應(yīng)中總是得到或失去電子而達(dá)到最外層最外層8電子的穩(wěn)定結(jié)構(gòu)����。電子的穩(wěn)定結(jié)構(gòu)。(2 2)不穩(wěn)定結(jié)構(gòu)不穩(wěn)定結(jié)構(gòu):( (如�����,如����,失去:失去: NaNa���、MgMg���、Al Al 得到:得到:F F、O O���、ClCl) )原子原子最外層電子數(shù)最外層電子數(shù)4時�����,容易得到電子時�����,容易得到電子在化學(xué)反應(yīng)中����,在化學(xué)反應(yīng)中,原子核原子核不發(fā)生變化的����,但不發(fā)生變化的,但原子的原子的最外層電子最外層電子可能會發(fā)生變化��??赡軙l(fā)生變化。金屬單質(zhì)Na�、Mg能分別與非金屬單質(zhì)O2、Cl2反應(yīng)生成氧化物和氯化物
6�、,請寫出這些氧化物和氯化物的化學(xué)式����。 元素化合價原子最外層電子數(shù)目失去(或得到)電子的數(shù)目Na1Mg2O6Cl-1根據(jù)Na、Mg�����、O����、Cl原子在反應(yīng)中失去或得到電子的數(shù)目和該原子的最外層電子數(shù)目,推斷其氧化物和氯化物中元素的化合價�����,將結(jié)果填入下表: 一些元素的原子得失電子的情況Na2O、MgO����、NaCl�����、MgCl2 元素種類元素種類 得失電子得失電子 化合價化合價 數(shù)數(shù) 值值 金金 屬屬 活潑非金屬活潑非金屬 失電子失電子得電子得電子正正 價價失電子失電子數(shù)數(shù)負(fù)負(fù) 價價得電子數(shù)得電子數(shù)原子的構(gòu)成是怎樣的?原子原子原子核原子核核外電子核外電子 質(zhì)子質(zhì)子 中子中子對于離子呢 �����?(離子和原子如何區(qū)別
7�����、)1個質(zhì)子帶一個單位正電荷個質(zhì)子帶一個單位正電荷1個電子帶一個單位負(fù)電荷個電子帶一個單位負(fù)電荷中子不帶電中子不帶電質(zhì)子數(shù)質(zhì)子數(shù)=核外電子數(shù)核外電子數(shù)呈電中性呈電中性1. 原子的電性原子的電性 �����?思考:思考:核電荷數(shù)核電荷數(shù)= 離子的電性����?離子的電性��?陽離子:質(zhì)子數(shù)電子數(shù)陽離子:質(zhì)子數(shù)電子數(shù) 質(zhì)子數(shù)質(zhì)子數(shù)=電子數(shù)電子數(shù)+電荷絕對值電荷絕對值陰離子:質(zhì)子數(shù)電子數(shù)陰離子:質(zhì)子數(shù)電子數(shù) 質(zhì)子數(shù)質(zhì)子數(shù)=電子數(shù)電子數(shù)-電荷絕對值電荷絕對值XAZ元素符號元素符號質(zhì)量數(shù)質(zhì)量數(shù) 質(zhì)子數(shù)質(zhì)子數(shù)(核電荷數(shù)(核電荷數(shù) )質(zhì)量數(shù)質(zhì)量數(shù) =質(zhì)子數(shù)質(zhì)子數(shù)(Z)+中子數(shù)中子數(shù)(N)集中在原子核集中在原子核2. 原子的質(zhì)量原子
8�、的質(zhì)量 ���? 對于離子呢���?對于離子呢?一個質(zhì)子的相對質(zhì)量是:一個質(zhì)子的相對質(zhì)量是:1.007一個中子的相對質(zhì)量是:一個中子的相對質(zhì)量是:1.008一個電子的相對質(zhì)量是:一個電子的相對質(zhì)量是:1/1836思考:思考:(A)ab+ dXec+-a代表質(zhì)量數(shù)代表質(zhì)量數(shù)b代表質(zhì)子數(shù)或核電荷數(shù)代表質(zhì)子數(shù)或核電荷數(shù)c代表離子所帶電荷數(shù)代表離子所帶電荷數(shù)d代表化合價代表化合價e代表原子個數(shù)代表原子個數(shù)a���、b�����、c���、d、e 各表示什么����?各表示什么?離子離子3. 原子的體積原子的體積 ����?由核外電子運動范圍決定�����,如果把它看成由核外電子運動范圍決定���,如果把它看成一個球,半徑約為一個球�,半徑約為10-10m很小很小1 1
9����、. .質(zhì)量數(shù)(質(zhì)量數(shù)(A) 質(zhì)子數(shù)(質(zhì)子數(shù)(Z) 中子數(shù)(中子數(shù)(N) 2.原子原子 :核電荷數(shù)核電荷數(shù) 質(zhì)子數(shù)質(zhì)子數(shù) 核外電子數(shù)核外電子數(shù)XAZ3. 陽離子陽離子 :核電荷數(shù)核電荷數(shù) 質(zhì)子數(shù)質(zhì)子數(shù) 核外電子數(shù)核外電子數(shù),maW4. 陰離子陰離子 :核電荷數(shù)核電荷數(shù) 質(zhì)子數(shù)質(zhì)子數(shù) 核外電子數(shù)核外電子數(shù)���,nbY原子核原子核核外電子核外電子質(zhì)子質(zhì)子中子中子原子原子XAZ總總 結(jié)結(jié) 核外電子數(shù)核外電子數(shù)a am m 核外電子數(shù)核外電子數(shù)b bn n1.以下說法正確的是以下說法正確的是A.原子是最小的粒子原子是最小的粒子B.所有原子都有中子所有原子都有中子C.原子呈電中性�����,所以原子不含電荷原子呈電中性
10�、���,所以原子不含電荷D.原子質(zhì)量主要集中在原子核上原子質(zhì)量主要集中在原子核上(D)(B)2.已知某元素相對原子質(zhì)量為已知某元素相對原子質(zhì)量為227���、中子數(shù)為中子數(shù)為138��,則質(zhì)子數(shù)為��,則質(zhì)子數(shù)為 A. 416 B. 89 C. 227 D. 2033.關(guān)于關(guān)于 Cl敘述錯誤的是敘述錯誤的是A.質(zhì)量數(shù)為質(zhì)量數(shù)為37 B.中子數(shù)為中子數(shù)為20C.電子數(shù)為電子數(shù)為17D.相對原子質(zhì)量為相對原子質(zhì)量為35.53717(D)4.某金屬原子符號為某金屬原子符號為 X��,該原子原子核內(nèi)����,該原子原子核內(nèi) 中子數(shù)與質(zhì)子數(shù)之差為中子數(shù)與質(zhì)子數(shù)之差為 A. 32 B. 67 C. 99 D. 16616667(A)5.
11��、下列粒子中與下列粒子中與NH4+具有相同質(zhì)子數(shù)和電具有相同質(zhì)子數(shù)和電 子數(shù)的是子數(shù)的是 A. Na+ B. F C. OH D. H2O (A) 6���、某微粒用����、某微粒用 Rn+表示���,下列關(guān)于該微粒的敘表示���,下列關(guān)于該微粒的敘 述中正確的是述中正確的是 A、所含質(zhì)子數(shù)����、所含質(zhì)子數(shù)=A-Z B���、所含中子數(shù)、所含中子數(shù)=A-Z C�����、所含電子數(shù)����、所含電子數(shù)=Z+n D、質(zhì)量數(shù)�、質(zhì)量數(shù)=Z+nZA7�、某元素的某種離子、某元素的某種離子X2-核外共有核外共有a個電子����,核個電子,核內(nèi)有內(nèi)有b個中子�����,表示該個中子��,表示該X原子的下列符號中正確原子的下列符號中正確的是的是XAbaa)(、XBba2a)()(�、X
12、C2ba2a)()(��、XD2ba2a)()(���、一切物質(zhì)都是由最小的不能再分的粒子一切物質(zhì)都是由最小的不能再分的粒子原原子構(gòu)成����。子構(gòu)成�����。 原子模型:原子是堅實的�����、不可再分的原子模型:原子是堅實的�����、不可再分的實心球?qū)嵭那颉?904湯姆生湯姆生提出了原子結(jié)構(gòu)的提出了原子結(jié)構(gòu)的 “葡萄干面包式模型葡萄干面包式模型”原子是一個平均分布著正電荷的陽極球�,其中均原子是一個平均分布著正電荷的陽極球,其中均勻鑲嵌著許多電子����,中和了電荷���,從而形成了中勻鑲嵌著許多電子,中和了電荷���,從而形成了中性原子�。性原子�。 原子由原子核和電子構(gòu)成原子由原子核和電子構(gòu)成,電子在核周圍做高速運動電子在核周圍做高速運動,就就像行星圍繞太陽運轉(zhuǎn)一樣。像行星圍繞太陽運轉(zhuǎn)一樣����。1911盧瑟福盧瑟福提出了原子的提出了原子的 “核式模型核式模型”丹麥物理學(xué)家玻爾丹麥物理學(xué)家玻爾1913年,丹麥物理學(xué)家����,丹麥物理學(xué)家玻爾玻爾提出的原子結(jié)構(gòu)模型����,提出的原子結(jié)構(gòu)模型,他認(rèn)為核外電子是他認(rèn)為核外電子是分層排布分層排布的��。的�。電電 子子 云云現(xiàn)代原子結(jié)構(gòu)學(xué)說現(xiàn)代原子結(jié)構(gòu)學(xué)說量子力學(xué)模型量子力學(xué)模型(1926年年)
 高中化學(xué)專題一 化學(xué)家眼中的物質(zhì)世界課件 蘇教版必修一原子結(jié)構(gòu)第一課時
高中化學(xué)專題一 化學(xué)家眼中的物質(zhì)世界課件 蘇教版必修一原子結(jié)構(gòu)第一課時