《新人教版高中化學必修一課時講義:第一章 第一節(jié) 第二課時 物質(zhì)的轉(zhuǎn)化含解析》由會員分享�,可在線閱讀,更多相關(guān)《新人教版高中化學必修一課時講義:第一章 第一節(jié) 第二課時 物質(zhì)的轉(zhuǎn)化含解析(8頁珍藏版)》請在裝配圖網(wǎng)上搜索��。
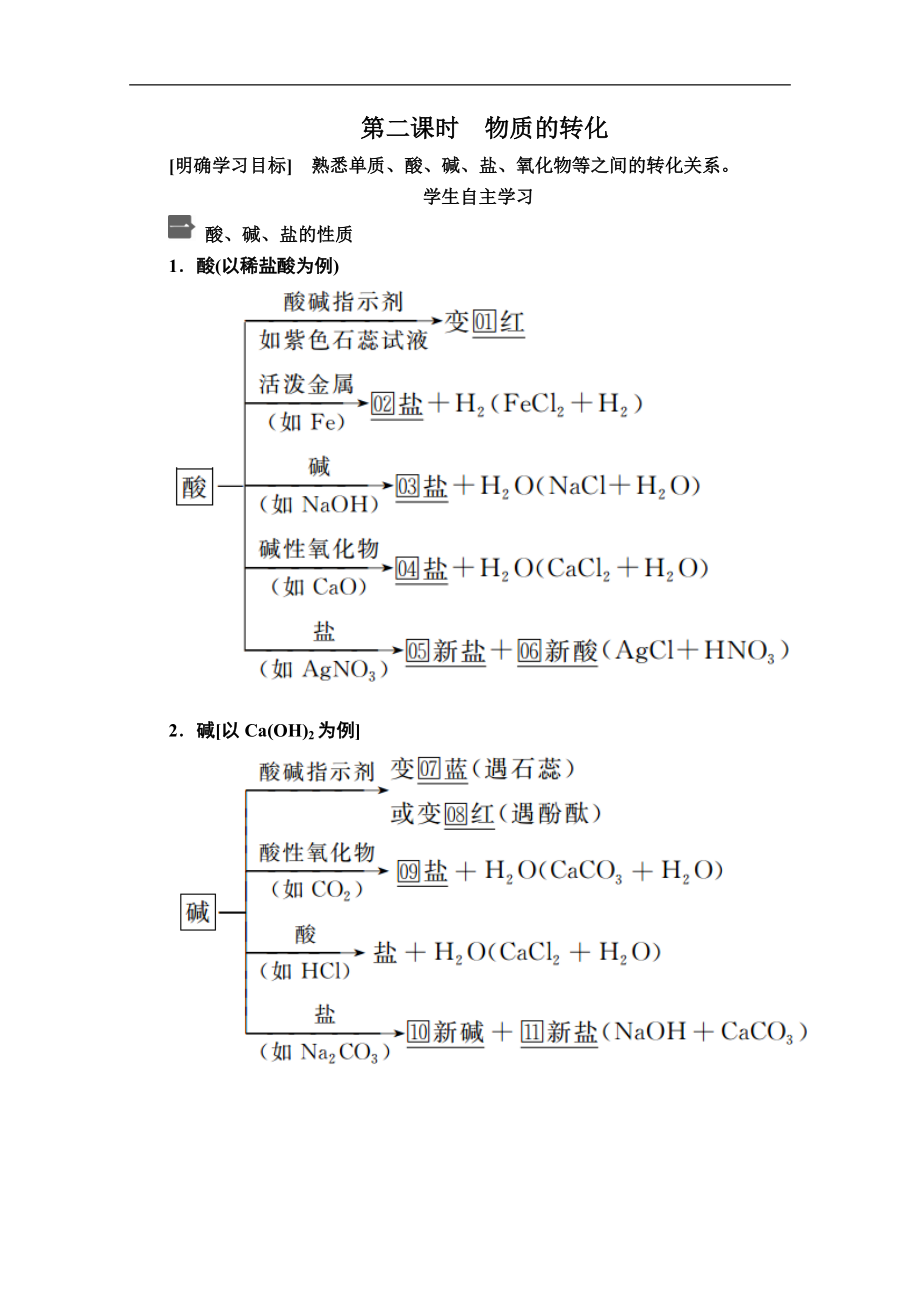
1�����、第二課時物質(zhì)的轉(zhuǎn)化明確學習目標熟悉單質(zhì)、酸����、堿、鹽����、氧化物等之間的轉(zhuǎn)化關(guān)系。學生自主學習 酸����、堿、鹽的性質(zhì)1酸(以稀鹽酸為例) 2堿以Ca(OH)2為例 物質(zhì)的轉(zhuǎn)化1在化學變化過程中����,元素是不會改變的�����,這是考慮如何實現(xiàn)物質(zhì)之間的轉(zhuǎn)化時最基本的依據(jù) 2實例寫出標號的化學反應方程式:2CaO2=2CaOCaOH2O=Ca(OH)2Ca(OH)2CO2=CaCO3H2OCO2CO2CO2H2O=H2CO3H2CO3Ca(OH)2=CaCO32H2O1為什么不同的酸(或堿)具有相似的化學性質(zhì)�?提示:盡管酸(或堿)不同,但它們的水溶液中都含有H(或OH)�,其相似的性質(zhì)實際上是H(或OH)的性質(zhì)。2純堿屬
2�、于堿嗎�?提示:純堿Na2CO3不是堿�,屬于碳酸鹽。課堂互動探究知識點一酸��、堿�����、鹽的性質(zhì)1酸����、堿的性質(zhì):酸與堿反應生成鹽和水;酸與堿性氧化物����、堿與酸性氧化物反應生成鹽和水;酸與金屬活動性順序表中排在氫前面的金屬反應生成鹽和H2��。2鹽的性質(zhì):鹽與酸(或堿�����、或鹽)只有產(chǎn)生沉淀�、氣體或H2O時才能反應。知識點二單質(zhì)��、氧化物、酸�、堿和鹽之間的轉(zhuǎn)化關(guān)系說明:上圖中的非金屬不包括氧氣和氫氣。某同學要在奧運五連環(huán)中填入物質(zhì)�����,使相連物質(zhì)間能發(fā)生反應�,不相連物質(zhì)間不能發(fā)生反應。你認為“五連環(huán)”中有空缺的一環(huán)應填入的物質(zhì)是()A硫酸鈉 B氧氣C二氧化碳 D氧化鈣批注點撥答案C練1下列各組物質(zhì)相互混合后��,不會發(fā)生反應
3�����、的是()ANa2SO4溶液和MgCl2溶液BNa2CO3溶液和稀硫酸CNaOH溶液和Fe2(SO4)3溶液DCa(OH)2溶液和鹽酸答案A解析物質(zhì)在溶液中是否能夠發(fā)生化學反應����,可根據(jù)是否生成沉淀�����、氣體或H2O來進行判斷�。Na2SO4和MgCl2溶液混合后既沒有沉淀、也沒有氣體和H2O生成�,故不反應����。練2如圖中����,“”表示相連的物質(zhì)間在一定條件下可以反應,“”表示丁在一定條件下通過置換反應可以轉(zhuǎn)化為乙�����。下面四組選項中�,符合圖示要求的是()答案C解析A項,H2SO4和Na2SO4�����、Na2SO4和NaOH����、NaOH和NaCl、NaCl和H2SO4不反應�;B項,BaCl2和KOH不反應��;D項����,Cu與HC
4��、l不發(fā)生置換反應生成CuCl2�����。C項中��,CH2OCOH2�����。方法規(guī)律(1)各類物質(zhì)的相互轉(zhuǎn)化關(guān)系圖并非無所不含����,有些規(guī)律未能體現(xiàn)�。(2)復分解反應的條件:能生成沉淀、氣體或水�。(3)金屬間發(fā)生置換反應的條件:金屬活動性強的置換弱的。判斷金屬與酸反應時:金屬必須排在H前面�;酸不可用硝酸����、濃硫酸�����。判斷金屬與鹽反應時:必須同時滿足“排在前面的金屬”和“可溶性鹽”兩個條件�。本課歸納總結(jié)單質(zhì)�、氧化物、酸�����、堿�、鹽之間的轉(zhuǎn)化關(guān)系學習效果檢測1將下列各組物質(zhì)按酸、堿�����、鹽的分類依次排列����,正確的是()A硫酸�����、純堿、石膏B硫酸��、燒堿�、膽礬C硫酸氫鈉、生石灰�����、醋酸鈉D磷酸����、熟石灰、苛性鈉答案B解析硫酸屬于酸��,純堿是Na
5��、2CO3��,屬于鹽�����,石膏屬于鹽����,A錯誤����;硫酸屬于酸����,燒堿是NaOH�,屬于堿,膽礬是五水硫酸銅��,屬于鹽��,B正確��;硫酸氫鈉屬于鹽��,生石灰屬于氧化物����,醋酸鈉屬于鹽,C錯誤��;磷酸屬于酸�,熟石灰屬于堿,苛性鈉是NaOH�����,屬于堿,D錯誤��。2實驗室中的藥品常按物質(zhì)的性質(zhì)����、類別等不同而有規(guī)律地放置。在做“酸的性質(zhì)”實驗時�����,實驗桌上部分藥品的擺放如圖所示����。某同學取用KOH溶液后應把它放回的位置是()答案D解析KOH屬于堿類物質(zhì),應與NaOH放在一起�����。3下列物質(zhì)一定是由三種元素組成的是()A氧化物 B堿 C酸 D鹽答案B解析堿一定是由H�、O、金屬元素(或N元素)三種元素組成的����。4下列物質(zhì)間的轉(zhuǎn)化可由一步反應完成的是
6����、(提示:SiO2既不溶于水也不與水反應)()ASiO2H2SiO3 BCu(OH)2Fe(OH)3CCaCO3Na2CO3 DCuCu(NO3)2答案D解析A項�����,酸性氧化物轉(zhuǎn)化為酸��,應按酸性氧化物水酸的反應形式直接轉(zhuǎn)化��,但SiO2與水不反應����,故SiO2不能由一步反應變?yōu)镠2SiO3�;B項,堿變?yōu)槠渌麎A��,應按堿鹽新堿新鹽的反應形式直接轉(zhuǎn)化��,Cu(OH)2不溶于水��,一般不能與鹽反應生成其他堿����,故Cu(OH)2不能由一步反應轉(zhuǎn)化為Fe(OH)3����;C項�,鹽變?yōu)槠渌},可能的反應形式為鹽堿新鹽新堿����、鹽酸新鹽新酸、鹽鹽新鹽新鹽��、鹽金屬新鹽新金屬�����,由于CaCO3難溶于水����,故它難與其他物質(zhì)反應轉(zhuǎn)變?yōu)橐兹苡谒?/p>
7、Na2CO3�����;D項����,金屬變?yōu)辂}�����,可能的反應形式為金屬酸鹽H2(強氧化性酸反應產(chǎn)生其他氣體)��、金屬鹽新金屬新鹽��,銅可與AgNO3溶液反應直接產(chǎn)生Cu(NO3)2�����。5依據(jù)現(xiàn)有知識分析判斷,下列反應不能發(fā)生的是()ANaOHKCl=NaClKOHBAgNO3HCl=AgClHNO3CNa2CO3Ca(OH)2=2NaOHCaCO3DBaCO32HNO3=Ba(NO3)2H2OCO2答案A解析酸�、堿、鹽之間發(fā)生反應的條件是生成沉淀�、氣體或水,由此可知只有A項中的反應不能發(fā)生��。6KOH是我國古代紡織業(yè)常用作漂洗的洗滌劑��。古代制取KOH的流程如下:上述流程中沒有涉及的化學反應類型是()A化合反應 B分解反
8��、應C置換反應 D復分解反應答案C解析該流程中發(fā)生的反應依次是:CaCO3CaOCO2(分解反應)�,CaOH2O=Ca(OH)2(化合反應),Ca(OH)2K2CO3=CaCO32KOH(復分解反應)��。7同一物質(zhì)按照不同的分類標準可以分為很多類別,按照物質(zhì)的成分對下列10種物質(zhì)進行分類:水空氣鐵二氧化碳硫酸熟石灰Ca(OH)2膽礬(CuSO45H2O)食鹽水堿式碳酸銅Cu2(OH)2CO3硫酸氫鈉(NaHSO4)(1)屬于混合物的是_ _�;(2)屬于氧化物的是_ _;(3)屬于堿的是_ _�����;(4)屬于酸的是_ _��;(5)屬于鹽的是_ _����;(6)屬于銅鹽的是_ _;(7)屬于鈉鹽的是_ _�����。答案(
9����、1)(2)(3)(4)(5)(6)(7)解析物質(zhì)可分為純凈物、混合物����。膽礬(CuSO45H2O)、Cu2(OH)2CO3����、NaHSO4都有固定的組成��,均為純凈物�����。食鹽水由NaCl和水兩種物質(zhì)組成����,屬于混合物��。酸����、堿����、鹽等都有明確的概念,可以根據(jù)物質(zhì)的分類進行判斷����。8在稀硫酸、二氧化碳��、銅片、食鹽����、生石灰、一氧化碳�、純堿、鐵片和木炭粉9種物質(zhì)間存在如圖所示關(guān)系��,給選擇適當?shù)奈镔|(zhì)��,使有連線的兩種物質(zhì)能發(fā)生反應����。(1)請推斷它們的化學式分別為:_;_�;_;_��;_����。(2)寫出下列物質(zhì)之間反應的化學方程式:和_;和_�����;和_;和_�����。答案(1)FeH2SO4CO2CaONa2CO3(2)FeH2SO4=FeSO4H2CaOH2SO4=CaSO4H2OH2SO4Na2CO3=Na2SO4H2OCO2CO2CaO=CaCO3解析據(jù)單質(zhì)能和酸發(fā)生化學反應�����,推知應為活潑金屬單質(zhì)�����,即為鐵�;而酸只有稀H2SO4,即為稀H2SO4����,則氧化物應為金屬氧化物��,即為CaO��,氧化物為酸性氧化物�,即為CO2;屬于鹽且既能與稀H2SO4反應,又能與CaO在水溶液中反應�����,則應為Na2CO3�。
 新人教版高中化學必修一課時講義:第一章 第一節(jié) 第二課時 物質(zhì)的轉(zhuǎn)化含解析
新人教版高中化學必修一課時講義:第一章 第一節(jié) 第二課時 物質(zhì)的轉(zhuǎn)化含解析